Namens de Werkgroep Lopen na CVA
PROF. DR. V.G.M. (VIVIAN) WEERDESTEYN
Hoogleraar Bewegingssturing en Revalidatie, Afdeling Revalidatie, Radboudumc en Sint Maartenskliniek, Nijmegen
DR. J.H. ( JORIK) NONNEKES
Revalidatiearts, Afdeling Revalidatie, Radboudumc en Sint Maartenskliniek, Nijmegen
DR. J.F.M. ( JUDITH) FLEUREN
Revalidatiearts, Roessingh, Centrum voor Revalidatie, Enschede
PROF. DR. J.H. ( JAAP) BUURKE
Hoogleraar Technologisch ondersteunde analyse van het menselijk bewegen, Universiteit Twente, afd. Biomedische signalen en systemen, Enschede; Roessingh Research and Development, Enschede
DR. H.J.R (HANNEKE) VAN DUIJNHOVEN
Revalidatiearts, Afdeling Revalidatie, Radboudumc en Sint Maartenskliniek, Nijmegen
PROF. DR. A.C.H. (SANDER) GEURTS
Hoogleraar Revalidatiegeneeskunde, Afdeling Revalidatie, Radboudumc en Sint Maartenskliniek, Nijmegen
Determinanten van loopvaardigheid
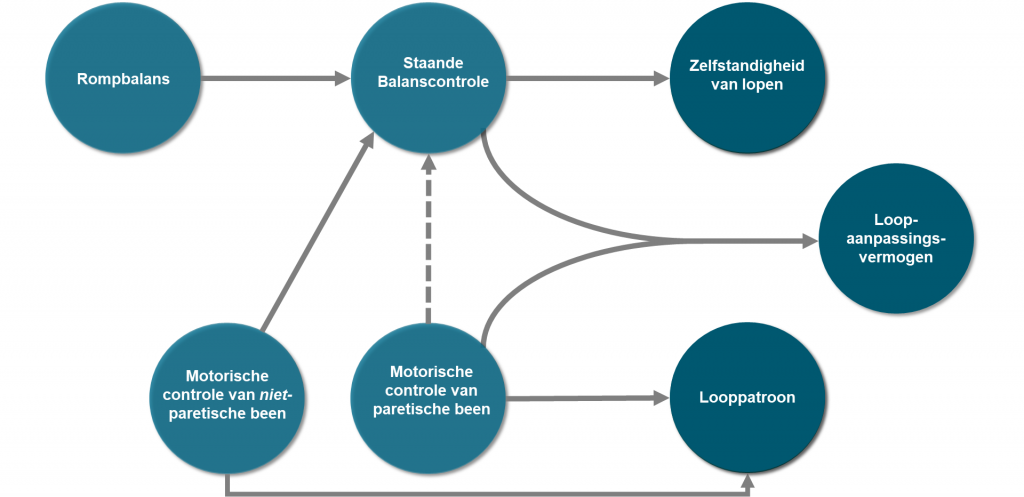
Voor een optimale efficiëntie en veiligheid van lopen zijn drie constructen te onderscheiden: zelfstandigheid van lopen, het looppatroon, en het loopaanpassingsvermogen (zie rechterzijde
figuur 1). Het theoretische framework beschrijft hoe balanscontrole (bovenste horizontale as) en motorische controle van de beide benen (onderste horizontale as) interacteren en gezamenlijk de loopvaardigheid bepalen.
Zelfstandigheid van lopen
Zelfstandig lopen wordt gedefinieerd als de vaardigheid om zich met of zonder hulpmiddel voorwaarts te kunnen bewegen in een rechtopstaande houding.2 Van alle mensen die initieel hun
loopvaardigheid verliezen na een CVA kan ongeveer 65% binnen een half jaar weer zelfstandig lopen.2 Het meeste functioneel herstel vindt plaats binnen drie maanden na het ontstaan van
het CVA.3 De kans dat in de chronische fase nog klinisch relevant functioneel herstel plaatsvindt is relatief klein.3 Voor het herwinnen van een zelfstandige loopvaardigheid is de balanscontrole in
staande houding de belangrijkste determinant.4,5 De staande balanscontrole
wordt op zijn beurt weer sterk bepaald door de mate waarin de romp kan worden gecontroleerd.6 Een goede rompcontrole is daarmee tevens een basisvoorwaarde voor zelfstandig lopen.4,5 Daarnaast speelt de motorische controle van het niet-paretische been een belangrijke rol (zie verder).
Balans houden in zit, stand, of tijdens beweging (bijvoorbeeld lopen) is een alledaagse, maar complexe taak. Hierbij interacteren motorische, sensorische en cognitieve factoren, welke functies
door een CVA vaak aangedaan zijn. Een CVA kan daarom een grote impact hebben op de balansvaardigheid. Voor een goede diagnostiek en behandeling van balansproblemen na een CVA is
het van belang om deze systematisch te ordenen. De term balans is feitelijk een paraplubegrip, waaronder drie verschillende vormen van balanscontrole onderscheiden kunnen worden:
steady-state, proactieve en reactieve balanscontrole.7
De steady-state (statische) balanscontrole is erop gericht om het lichaamszwaartepunt binnen het steunvlak te houden onder voorspelbare en onveranderlijke omstandigheden. Deze vorm van balanscontrole berust op basale evenwichtsreacties, waarbij gerichte spieractiviteit de uitwijkingen van het lichaamszwaartepunt controleert. Dit is een continu proces, aangezien we ons
flexibele lichaam per definitie niet in een perfect passieve evenwichtstoestand kunnen houden. Bij veel CVA-patiënten kenmerkt de steady-state balanscontrole tijdens staan zich door een toegenomen lichaamszwaai, vooral in de laterale richting, welke toeneemt tijdens visuele deprivatie of het uitvoeren van een cognitieve dubbeltaak.8 Regulerende spieractiviteit van het niet-paretische been levert daarbij een (veel) groter aandeel aan de balanscontrole dan die van het paretische
been, hetgeen overigens een effectieve compensatie vormt tijdens rustig staan. Hoewel de lichaamszwaai geleidelijk afneemt in de weken tot maanden na het CVA, blijft deze
regulatieasymmetrie bestaan.8
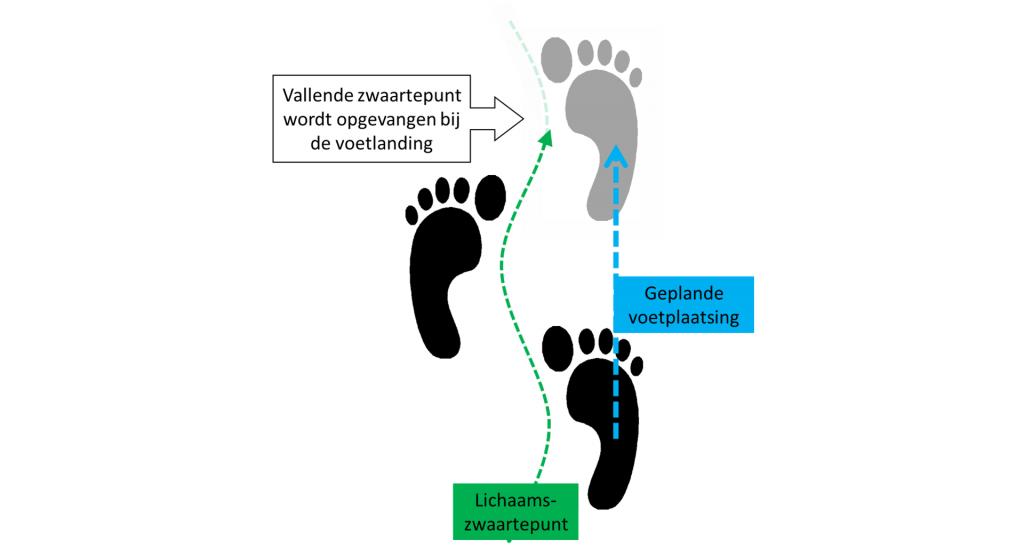
Proactieve balanscontrole betreft een patroon van spieractiviteit dat vooraf gaat aan de inzet van een vrijwillige beweging. Dit voorkómt dat het lichaam uit balans wordt gebracht door deze beweging. Naast motorische controle speelt cognitie hierbij een belangrijke rol. Het effect van de beweging op de balans moet immers worden voorspeld op basis van beschikbare kennis van en ervaring met de taak en worden vertaald naar het juiste patroon van voorbereidende spieractiviteit. Een mismatch hiertussen zal leiden tot een balansverstoring. Tijdens het lopen is proactieve balanscontrole essentieel voor de regulatie van voetplaatsing ten opzichte van het ‘vallende’ lichaamszwaartepunt (figuur 2). Na een CVA is deze koppeling tussen de bewegingen van het lichaamszwaartepunt en de voetplaatsing verstoord, vooral aan de paretische zijde. De paretische voet wordt gemiddeld meer naar lateraal geplaatst ten opzichte van de beweging van het lichaamszwaartepunt en dit gebeurt met een grotere variabiliteit.9 De combinatie van deze bevindingen duidt op het gebruik van een compensatiestrategie die de kans op balansverlies verkleint.
Reactieve balanscontrole betreft de actieve herstelreacties na een plotselinge en meestal onverwachte balansverstoring. Dit kunnen zowel externe (bijvoorbeeld een botsing) als interne verstoringen zijn. Interne verstoringen zijn vaak het gevolg van insufficiënte proactieve balanscontrole. In de detectie van balansverlies en de daarop volgende generatie van balansherstelreacties spelen zowel corticale als subcorticale hersengebieden een rol. Balansherstelreacties worden gekenmerkt door een multisegmentaal en synergistisch
patroon van spieractiviteit en vallen grofweg uiteen in twee categorieën: evenwichtsreacties (bijvoorbeeld enkel- en heupstrategieën) en stapreacties. In vergelijking met de verminderde
evenwichtsreacties zijn de gevolgen van een CVA op de kwaliteit van stapreacties veel prominenter. Vooral het kunnen zetten van een zijwaartse opvangstap met het paretische been is aangedaan,
hetgeen verklaart waarom valincidenten na een CVA vaak optreden naar de paretische zijde.10
De invloed van de motorische controle van het paretische been op de zelfstandigheid van het lopen is veel minder sterk dan de invloed van balanscontrole. Een goede motorische selectiviteit
van het paretische been is niet noodzakelijk om zelfstandigheid van lopen te bereiken, hetgeen blijkt uit het gegeven dat de ernst van het CVA geen voorspeller is voor het al dan niet herwinnen
van zelfstandige loopvaardigheid.3 Mits op de paretische zijde voldoende steun kan worden genomen, kan de balans voor het grootste deel worden gereguleerd vanuit de romp en gecompenseerd door het niet-paretische been8 (zie figuur 1). De negatieve invloed van verlies van motorische controle van het paretische been wordt vooral gezien bij balansverstoringen waarvoor een stapreactie nodig is om niet te vallen.11 Hiermee bepaalt de motorische controle van het paretische been dus niet zo zeer óf iemand zelfstandig kan staan en lopen, maar wel of iemand ook
veilig kan staan en lopen onder uitdagende omstandigheden (zie loopaanpassingsvermogen).
Looppatroon
Het looppatroon wordt gekenmerkt door een opeenvolging van bewegingen van de lichaamssegmenten tijdens de verschillende fasen van de loopcyclus. Hiervoor zijn voldoende spierkracht, voldoende bewegingsuitslag in voet-, enkel-, knie- en heupgewrichten, adequate sensibele input en een normale spiertonus van belang. Daarnaast is een verfijnde afstemming van activatie en ontspanning van romp-, onderbeen- en bovenbeenspieren aan beide zijden van het lichaam (selectiviteit van aansturing) essentieel voor een efficiënt en symmetrisch looppatroon. Het lopen wordt aangestuurd vanuit verschillende niveaus in het centraal zenuwstelsel: ruggenmerg, hersenstam, subcorticale kernen en hersenschors. De piramidebaan (corticospinale baan) speelt een
belangrijke rol bij het verfijnd aansturen van de spieren tijdens het lopen. Bij een beschadiging van de piramidebaan na een CVA treedt er waarschijnlijk deels compensatie op via het cortico-reticulospinale baansysteem, maar deze ‘lagere’ aansturing heeft als nadeel dat afzonderlijke spieren minder verfijnd aan en uit kunnen worden gezet. Deze verminderde motorische controle
van het paretische been uit zich in het klassieke looppatroon na een CVA, gekenmerkt door een zwakke voetheffing en voorvoet landing, knie-overstrekking in de standfase, verminderde afzet,
en verminderde knie- en heupflexie met ‘circumductie’ tijdens de zwaaifase. De motorische controle van het paretische been is in belangrijke mate bepalend voor het looppatroon. Dit zal in detail
worden uitgewerkt in het derde artikel van deze reeks.
Loopaanpassingsvermogen
Het loopaanpassingsvermogen betreft de vaardigheid om het lopen te kunnen aanpassen aan de eisen die de omgeving stelt (bijvoorbeeld het vermijden van obstakels) en berust op een complexe
interactie tussen de motorische controle van beide benen en de balanscontrole (zie figuur 1). Omdat men dergelijke situaties buitenshuis veelvuldig tegenkomt kan het loopaanpassingsvermogen
worden beschouwd als het ultieme revalidatiedoel gericht op volledig zelfstandige mobiliteit (zowel binnen- als buitenshuis). Het gaat er hierbij niet alleen om óf iemand in staat is te variëren in het looppatroon (bijvoorbeeld in snelheid, richting, staplengte/breedte/hoogte), maar vooral of deze variaties in de alledaagse context adequaat kunnen worden aangewend. Vaak is hierbij sprake van een zekere tijdsdruk; denk bijvoorbeeld aan een huisdier dat plotseling voor de voeten loopt. Onder een adequate uitvoering wordt verstaan dat het looppatroon kan worden aangepast aan de taak en omgeving en dat daarbij tevens de balans wordt behouden. Het betreft primair een vorm van
proactieve balanscontrole, echter hierbij wordt het verfijnde samenspel tussen de beweging van het lichaamszwaartepunt en de voetplaatsing (zoals geschetst in figuur 2) verder uitgedaagd. Daardoor neemt het risico op interne balansverstoringen toe, zodat tevens de reactieve balanscontrole moet worden aangesproken. Tijdens dergelijke complexe dynamische taken kan het niet-paretische been veel minder compenseren voor de verminderde sturing door het paretische been dan tijdens rustig staan en ongestoord lopen. Daarom is lopen in het dagelijkse leven zelfs voor goed herstelde patiënten na een CVA nog vaak een uitdagende taak die veel (mentale en fysieke) inspanning vraagt.
Nawoord
In dit artikel werd aan de hand van een theoretisch framework uiteengezet hoe afwijkingen in balanscontrole en motorische controle van beide benen gezamenlijk de loopvaardigheid na een
CVA bepalen. Een belangrijke aantekening hierbij is dat dit framework zich richt op de motorische problematiek en daarmee een vereenvoudiging betreft van de vaak complexe problematiek na
een CVA. Bij het vaststellen van de behandelstrategie kunnen in de praktijk uiteraard ook andere factoren (bijvoorbeeld cognitie en belastbaarheid) een rol spelen. In de vervolgartikelen zal worden
besproken hoe revalidatiebehandeling gericht op het verbeteren van loopvaardigheid kan worden vormgeven langs de lijnen zoals geïntroduceerd in dit framework.
Referenties
- Kouwenhoven M, Fengler RKB, Schiemanck SK, Fleuren JFM. Diagnostiek en behandeling van verminderde loopvaardigheid na CVA. NTR. 2017;39:32-4.
- Preston E, Ada L, Dean CM, Stanton R, Waddington G. What is the probability of patients who are nonambulatory after stroke regaining independent walking? A systematic
review. Int J Stroke. 2011;6:531-40 - Kollen B, van de Port I, Lindeman E, Twisk J, Kwakkel G. Predicting improvement in gait after stroke: A longitudinal prospective study. Stroke. 2005;36:2676-80
- Kollen B, Kwakkel G, Lindeman E. Longitudinal robustness of variables predicting independent gait following severe middle cerebral artery stroke: A prospective cohort
study. Clin Rehabil. 2006;20:262-8 - Veerbeek JM, Van Wegen EE, Harmeling-Van der Wel BC, Kwakkel G, Investigators E. Is accurate prediction of gait in nonambulatory stroke patients possible within 72
hours poststroke? The epos study. Neurorehabil Neural Repair. 2011;25:268-74 - Verheyden G, Vereeck L, Truijen S, Troch M, Herregodts I, Lafosse C, et al. Trunk performance after stroke and the relationship with balance, gait and functional ability.
Clin Rehabil. 2006;20:451-8 - Shumway-Cook A, Woollacott MH. Motor control: Translating research into clinical practice. Wolters Kluwer; 2017.
- de Haart M, Geurts AC, Huidekoper SC, Fasotti L, van Limbeek J. Recovery of standing balance in postacute stroke patients: A rehabilitation cohort study. Arch Phys Med
Rehabil. 2004;85:886-95 - Stimpson KH, Heitkamp LN, Embry AE, Dean JC. Post-stroke deficits in the step-by-step control of paretic step width. Gait Posture. 2019;70:136-40.
- Weerdesteyn V, De Niet M, Van Duijnhoven HJR, Geurts ACH. Falls in individuals with stroke. J Rehabil Res Dev. 2008;45:1195-1214.
- de Kam D, Heeren A, Roelofs JMB, Geurts ACH, Weerdesteyn V. Impaired ability to sustain balance perturbations in people with chronic stroke and its association with leg
and trunk motor function. https://ispgr.org/wp-content/uploads/2018/10/2017Abstracts.pdf, pagina 314.
Dit artikel verscheen in het Nederlands Tijdschrift voor Revalidatiegeneeskunde: Jaargang 44, Nummer 1, Februari 2022

Gerelateerde artikelen NTR

Herstel van loopvaardigheid na een CVA

Cognitieve screening en diagnostiek na een beroerte: het kan beter

Voorspelmodel van Rijndam Revalidatie geeft inzicht in herstel arm- handfunctie
Gerelateerde artikelen Revalidatie Magazine

‘Het onschuldige imago van lachgasgebruik moet verdwijnen’

Op zoek naar de geschikte game

