Innovatie
Er is een behoefte bij Clinics in Revalidatie (CIR) om patiënten meer te betrekken bij de besluitvorming rondom indicatiestelling voor pijnrevalidatie. Naast de reeds bestaande voorlichting door de revalidatiearts kunnen patiënten worden betrokken door uitkomstgericht te kijken. Machine learning kan worden gebruikt om gepersonaliseerde predictieprofielen te bouwen die het proces van samen beslissen ondersteunen. Deze modellen moeten alleen begrijpelijker worden gemaakt voor de revalidatiearts om bruikbaar te zijn als beslishulp.
Auteurs
J.S. ( JAN) GROENEWEGEN
Revalidatiearts Clinics in Revalidatie (CIR) Rotterdam, Nederland
PROF. DR. R.J.E.M. (ROB) SMEETS
Hoogleraar en revalidatiearts, Clinics in Revalidatie (CIR) Eindhoven, Nederland; department of Rehabilitation Medicine, Care and Public Health Research Institute (CAPHRI); Faculty of Health, Life Sciences and Medicine, Maastricht University, Nederland; Pain in Motion International Research Group (PiM), Brussel, België
F. (FREDRICK) ZMUDZKI
Promovendus department of Rehabilitation Medicine, Care and Public Health Research Institute CAPHRI), Faculty of Health, Life Sciences and Medicine, Maastricht University, Maastricht, Nederland; directeur Epoque consulting, Sydney Australë; senior gezondheidseconoom Social Policy Research Centre, University of New South Wales Sydney, Australië
Kunstmatige intelligentie of simpelweg ‘AI’ van het Engelse artificial intelligence is het vertonen van mensachtige intelligentie door machines. Intelligentie van machines kan vergeleken worden met menselijke cognitieve functies zoals perceptie, redeneren, talige functies en leren. Vele AI-innovaties zijn toepassingen van machine learning.

Machine learning
Machine learning, het leren van machines, kan, zoals het menselijk leren, beschreven worden volgens verschillende niveaus. Het criterium hierbij is de mate van menselijke bemoeienis bij het proces van leren. Onder andere wordt onderscheid gemaakt tussen supervised en unsupervised leren. Supervised learning betreft het vermogen van een algoritme om data nauwkeurig te classificeren.
‘Het proces van samen
beslissen ondersteunen met hulp
van machine learning’
Voorbeelden van dit soort algoritmen zijn classificatieregels, decision trees en regressietechnieken. In zorgapplicaties gaat het doorgaans om een binaire classificatie bijvoorbeeld een therapeutisch doel wel of niet behaald, aan- of afwezigheid van een aandoening bij diagnostiek. Supervised learning wordt gebruikt om predictiemodellen te bouwen. Dit zijn modellen die een bepaalde uitkomst of gebeurtenis voorspellen. Binnen de geneeskunde worden dergelijke modellen ontwikkeld om klinische besluitvorming, bijvoorbeeld samen beslissen met de patiënt, te ondersteunen en verbeteren. Unsupervised learning betreft het zoeken naar associaties of patronen in de data zonder dat een eindclassificatie gedefinieerd is.
Innovatie in de pijnrevalidatie
Bij Clinics in Revalidatie (CIR) zijn gestructureerde data uit het elektronisch patiëntendossier (EPD) gebruikt om een predictiemodel te bouwen. Het doel is om een gepersonaliseerde predictie te maken van uitkomsten die betekenisvol zijn voor de patiënt met pijn. Een dergelijke predictie zou de revalidatiearts kunnen meenemen in het gesprek met de patiënt tijdens de screening voorafgaand aan pijnrevalidatie. Initiële stappen in 2018 zijn geweest om data onafhankelijk en betrouwbaar te structureren binnen het EPD en om een dataset te definiëren. Voor machine learning zijn gestructureerde data van goede kwaliteit belangrijk voor het maken van betrouwbare predicties. Bij de ontwikkeling van het predictiemodel zijn verplichte en facultatieve onderdelen van de Nederlandse Dataset Pijnrevalidatie (NDP) gebruikt, aangevuld met nog enkele door de onderzoekers en CIR zinvol geachte vragenlijsten en performance-taken.
De interventie die CIR merendeels aanbiedt is systematisch beschreven met behulp van het TIDIer checklist.1 Vervolgens werd onderzocht of het pijnrevalidatie behandelprogramma bij CIR effectief is en of de effecten tot een jaar na einde behandeling behouden blijven.2
‘Ontwikkeling van predictiemodel
met data uit EPD en NDP voor
gepersonaliseerde predictie’
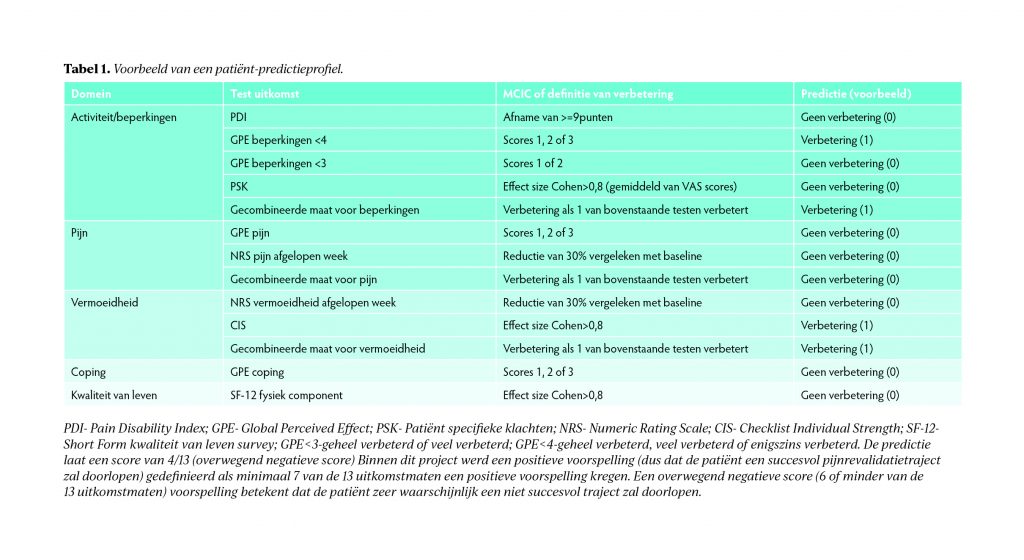
Het ontwikkelen van een predictiemodel is mede mogelijk gemaakt dankzij een onderzoeksubsidie voor het ontwikkelen van een dergelijk model voor mensen met chronische pijn en die ook artrose hebben. Een groep van experts is in eerste instantie bijeengekomen om uitkomsten en de klinische relevante verandering (de zogenaamde minimally clinical important change (MCIC)) die nodig is om van een succesvolle interventie te kunnen spreken aan de hand van literatuuronderzoek vast te stellen. De primaire en secundaire uitkomstmaten zoals gedefinieerd in de NDP zijn hierbij als uitgangspunt genomen.3 Deze uitkomsten zijn allemaal aanwezig in de dataset van CIR. Zo zijn 13 uitkomsten gedefinieerd over vijf uitkomstdomeinen (activiteiten, pijn, vermoeidheid, coping en kwaliteit van leven). De 13 uitkomsten zijn binair gedefinieerd (wel/geen verbetering) aan de hand van verandering in vragenlijstscores tussen nulmeting (intake) en eindmeting (evaluatie bij tien weken). De verandering moet gelijk of groter zijn dan de MCIC om te voldoen aan de definitie van ‘wel verbetering’.
De volgende stap was de keuze hoe het model te bouwen. Er zijn grofweg twee mogelijkheden: de klassieke manier of door middel van machine learning. De klassieke manier maakt gebruik van regressietechnieken (multivariate regressie) en vereist kennis van prognostische factoren die in het causale pad van de prognose liggen. In het kader van de eerdergenoemde subsidie heeft een groep van patiënten, clinici en onderzoekers tijdens een consensusmeeting bepaald welke factoren mogelijk voorspellend zijn voor de uitkomsten van pijnrevalidatie. Hiertoe heeft eerst een uitgebreide literatuurstudie plaatsgevonden en vervolgens is deze groep tot een definitieve selectie gekomen.4 Alle tijdens dit proces geselecteerde prognostische factoren bleken in de CIR-dataset aanwezig te zijn.
Echter, in dit proces ontstond de behoefte om te kijken naar meer factoren dan die op basis van bestaande literatuur zijn onderzocht en middels consensus zijn vastgesteld. Machine learning was daarom een aantrekkelijke keuze. Bij machine learning kan men de causaliteitseis loslaten en breder kijken naar de invloed van meerdere factoren, zowel demografisch als klinisch. Een groot deel van de klinische data wordt verkregen middels door patiënt ingevulde vragenlijsten (PROMS), data die verzameld worden op basis van input van de revalidatiearts en zijn/haar teamleden (WPN-classificatie, wel/niet indicatie voor EMDR), performance-testen (bijvoorbeeld vijf keer zitten-opstaan test) maar ook locatie van CIR waar de behandeling werd uitgevoerd. Uiteindelijk is een predictiemodel gebouwd met 13 uitkomsten, elk met de 30 meest bijdragende ‘prognostische’ factoren (of features) aan een accurate classificatie (wel versus niet verbeterd). Het proces van selecteren van dergelijke factoren voor optimalisatie van een algoritme heet ‘feature selectie’. Deze factoren correleren in meer of mindere mate met de uitkomst van de classificatie en ze worden berekend door de machine learning software. Het algehele model bestaat dus eigenlijk uit meerdere algoritmes (één algoritme per uitkomst). In tabel 1 is een voorbeeld van een predictieprofiel met 13 uitkomsten weergegeven.
De volgende stap was interne validatie van het model. In dit proces is dat op meerdere manieren gebeurd. Zie tabel 2 voor nadere uitleg over deze stap. Externe validatie vindt inmiddels plaats, deels binnen CIR op een nieuwe dataset van ca. 1.900 patiënten van 2022-23 (inclusief patiënten van nieuwe locaties van CIR) en deels bij andere instellingen buiten CIR (zie verderop).

Wat vindt de revalidatiearts?
Bij CIR is recent een kwalitatieve studie5 verricht om de perceptie en acceptatie van het predictiemodel als beslishulp bij revalidatieartsen, een stafarts en physician assistants te onderzoeken. Tijdens een medische stafvergadering is een focusgroep-sessie gehouden, opgenomen, getranscribeerd en geanalyseerd middels thematische contentanalyse. De revalidatiearts zou bereid moeten zijn om het predictiemodel te gebruiken om te komen tot een succesvolle implementatie. Echter uit een rapport6 over gebruik van uitkomstinformatie in de zorg is gebleken dat zorgverleners zelden kijken naar beschikbare informatie over predicties tijdens een intake. De zorgverleners gaven liever informatie aan patiënten gebaseerd op eigen kennis en ervaringen. Predictie-informatie werd vooral gebruikt om de eigen besluiten van zorgverleners te ondersteunen.
De volgende belangrijke thema’s kwamen tijdens de focusgroep naar voren:
- Clinici hebben een behoefte om het model beter te begrijpen, met name de basis waarop de predictie tot stand kwam, hoe de predictie te interpreteren.
- Er is een behoefte bij de deelnemers om een instructie te krijgen over hoe de informatie van de predictie over te brengen aan de patiënt.
- Er zijn zorgen dat de predictie bepalend zou zijn voor de besluitvorming rondom inclusie voor pijnrevalidatie, hoewel uitgelegd is dat dit niet de intentie achter de innovatie is geweest. De revalidatiearts zal altijd autonoom blijven om in samenspraak met de patiënt besluiten te nemen over wel of niet indiceren voor een pijnrevalidatietraject.7
- Er zijn zorgen dat het tonen van predictie-informatie aan patiënten een verstorende werking zou hebben in de communicatie over pijn met de patiënt. In dit verband werd ook een mogelijk nocebo effect genoemd.
Hoe verder?
Voor de doorontwikkeling van het predictiemodel als digitale beslissingsondersteuning voor de revalidatiearts werkzaam in de pijnrevalidatie is het belangrijk om de genoemde thema’s mee te nemen in een volgend prototype. Er kan inzicht worden gegeven in de factoren die tot een predictie hebben geleid. Aangezien deze niet per se binnen het causale pad liggen kan dit toch de neiging geven aan clinici om iets aan deze factoren te willen veranderen vanuit het oogpunt van zorgverbetering. De vraag is dan of dergelijke interventies effectief zijn. Een ander effect kan zijn een verandering in prestaties van het predictiemodel. De algoritmen in het model zullen onderhouden moeten worden, bijvoorbeeld door re-kalibratie waar nodig. Een instructie zal onderdeel moeten zijn van de implementatie: instructie over hoe het model te interpreteren, hoe het te communiceren met patiënten, rekening houdend met ongewenste, onbedoelde effecten. Voor clinici die het willen kan de kans worden aangeboden om het predictiemodel uit te proberen in de dagelijkse zorg en er ervaringen mee op doen. Er kan dan bepaald worden of en hoe dit een invloed heeft op de besluitvorming. Initiële ervaringen op één van de CIR-locaties laat zien dat patiënten deze aanvullende informatie waarderen en meer vertrouwen kunnen krijgen in de deskundigheid van de revalidatiearts.
Naast bovenstaande strategieën zal er voldaan moeten worden aan een aantal technische en juridische aspecten. Naast de interne validatie moet er nog een deel van de externe validatie van het predictiemodel worden gedaan. Hiervoor zijn data nodig van andere centra waar pijnrevalidatie wordt aangeboden. Dit is vanuit zorgperspectief noodzakelijk maar het zal ook een aanvraag in het kader van het Medical Device Regulation faciliteren. Als belangrijke technische voorwaarde investeert CIR nu in een datawarehouse waarbij het doen van observationeel onderzoek en machine learning als processen geautomatiseerd zijn. Dit zal de informatiebeveiliging ten goede komen en routinematig gebruik van de predictie mogelijk maken.
Referenties
- Breugelmans L, Scheffer E, Beckers L, Oosterwijk RFA, Nijland G, Smeets R. Systematic description of an interdisciplinary multimodal pain treatment programme for patients with chronic musculoskeletal pain, using the TIDieR checklist. BMC Res Notes 2022;15(1):320. doi:10.1186/s13104-022-06211-z
- Breugelmans L, Smeets RJ, Köke AJA, Winkens B, Oosterwijk RFA, Beckers L. Outpatient interdisciplinary multimodal pain treatment programme for patients with chronic musculoskeletal pain: a longitudinal cohort study. Disabil Rehabil 2024:1-12. doi:10.1080/09638288.2024.2364822
- Köke AJ, Smeets RJ, Schreurs KM, van Baalen B, de Haan P, Remerie SC, Schiphorst Preuper HR, Reneman MF. Dutch Dataset Pain Rehabilitation in daily practice: Content, patient characteristics and reference data. Eur J Pain. 2017;21(3):434-44. doi:10.1002/ejp.937
- Vervullens S, Breugelmans L, Beckers L, van Kuijk SM, van Hooff M, Winkens B, Smeets RJ. Clinical prediction model for interdisciplinary biopsychosocial rehabilitation in osteoarthritis patients. Eur J Phys Rehabil Med. 2024;60(1):84-94. doi:10.23736/S1973-9087.23.08071-1
- Groenewegen J. Clinician acceptance of a personalized predictive profile for use as a decision aid. Amsterdam: Universiteit van Amsterdam; 2024.
- Arends D, van Kooij Y, Loos N, Selles R, Veltkamp J, Wouters R. Uitkomstinformatie in de dagelijkse zorg: van verzamelen naar gebruiken. Erasmus Medical Center; 2022. https://projecten.zonmw.nl/sites/zonmw/files/typo3-migrated-files/05160472110006_Rapport_Uitkomstinformatie_in_de_dagelijkse_zorg_van_verzamelen_naar_gebruiken_voor_beleidsmakers.pdf
- Zmudzki F, Smeets R. Machine learning clinical decision support for interdisciplinary multimodal chronic musculoskeletal pain treatment. Front Pain Res (Lausanne). 2023;4:1177070.
Gerelateerde artikelen NTR

Stap voor stap en samen op weg naar passende AI in de revalidatiezorg

Dokter AI: Wie is er beter in het beantwoorden van klinische vragen, de arts of AI?

‘De belangrijkste vraag: is technologie überhaupt de oplossing voor het probleem?’

Thuis meten van dystonie bij kinderen
Gerelateerde artikelen Revalidatie Magazine

Hybride revalidatie in Kennemerland
E-Revalidatie: doelgericht samenwerken aan effectieve e-health-toepassingen

Een app en ondersteuning geven patiënt Rob (73) de regie over de behandeling van ALS


