Inspanningsintolerantie en post-exertionele malaise bij patiënten met post-COVID syndroom
Patiënten met post-COVID syndroom lijden aan vermoeidheid, inspanningsintolerantie en post-exertionele malaise. Post-exertionele malaise is de verergering van klachten na fysieke, cognitieve of mentale inspanning, waardoor sommige vormen van revalidatie en fysiotherapie averechts werken voor het herstel van deze patiënten. In dit artikel wordt de huidige wetenschappelijke stand van zaken op het gebied van de pathofysiologie van post-COVID syndroom weergegeven, in het bijzonder de onderliggende oorzaken van post-exertionele malaise.
Auteurs
E.A. (ELLEN) BREEDVELD MSC
Fysiotherapeut, Ziekenhuis Gelderse Vallei, Ede; Faculteit Gedrag- en Bewegingswetenschappen, Vrije Universiteit Amsterdam, Amsterdam
B. (BRENT) APPELMAN MSC
PhD student, Centrum voor Experimentele en Moleculaire Geneeskunde, afdeling infectieziekten, Amsterdam UMC locatie AMC, Amsterdam
K. (KASPER) JANSSEN PHD
Sportarts, DeSportarts Utrecht, afdeling sport- en leefstijlgeneeskunde, Julius Gezondheidscentra, Leidsche Rijn Centrum, Utrecht
PROF. DR. M. (MICHÈLE) VAN VUGT
Professor bestrijding infectieziekten, afdeling Infectieziekten en Tropengeneeskunde, Amsterdam UMC locatie AMC, Amsterdam
R.C.I. (ROB) WÜST PHD
Universitair docent, faculteit Gedrag- en Bewegingswetenschappen, Vrije Universiteit Amsterdam, Amsterdam
Hoewel de meerderheid van de mensen die besmet zijn met het SARS-CoV-2 virus binnen enkele weken herstelt, houdt een subgroep lange-termijn symptomen. Symptomen bij patiënten met long COVID, post-acute sequelae of COVID of post-COVID syndroom (PCS) bestaan uit onder andere ernstige cognitieve problemen (hersenmist), vermoeidheid, inspanningsintolerantie, autonome disregulatie, posturele orthostatische tachycardie syndroom (POTS), orthostatische intolerantie, en post-exertionele malaise (PEM). PEM is de langdurige verergering van klachten die binnen drie dagen ontstaat na fysieke, cognitieve of mentale inspanning boven een onbekende, individuele drempel; dit kan weken tot maanden aanhouden1,2 en voor een terugval zorgen. PEM is een belangrijke factor waardoor patiënten niet kunnen deelnemen aan de maatschappij. De pathofysiologie van PEM is onbekend, en anders dan de pathofysiologie van acute inspanningsintolerantie. Door het optreden van PEM werken sommige vormen van revalidatie en fysiotherapie averechts waardoor patiënten in een zogenaamde push-and-crash-cyclus kunnen komen. PEM komt ook voor bij andere post-infectieuze ziekten en Myalgische Encefalomyelitis/Chronisch Vermoeidheidssyndroom (ME/CVS).1,3 Momenteel wordt de diagnose post-COVID syndroom gesteld door het uitsluiten van alternatieve diagnoses, maar vanwege de overlap worden ook verschillende diagnostische criteria gebruikt voor ME/CVS, zoals de NICE richtlijn (2021).4 Binnen het post-COVID syndroom zijn er waarschijnlijk subgroepen van patiënten, met PEM als grote gemene deler.5 Het is echter belangrijk om binnen het post-COVID syndroom onderscheid te maken tussen patiënten met en zonder PEM. Binnen de groep patiënten zonder PEM kan er een onderscheid gemaakt worden tussen patiënten die wel en niet opgenomen zijn geweest in het ziekenhuis. Deze eerste groep kan (zeer) lang na ontslag nog restsymptomen, zoals vermoeidheid en inspanningsintolerantie houden. Duur- en krachttraining kunnen bij deze patiënten zonder PEM wel leiden tot een verbetering van fysieke en cognitieve functies en verbetering van zelfredzaamheid. Echter, deze positieve resultaten van revalidatie zijn niet zonder meer van toepassing op patiënten met PEM.
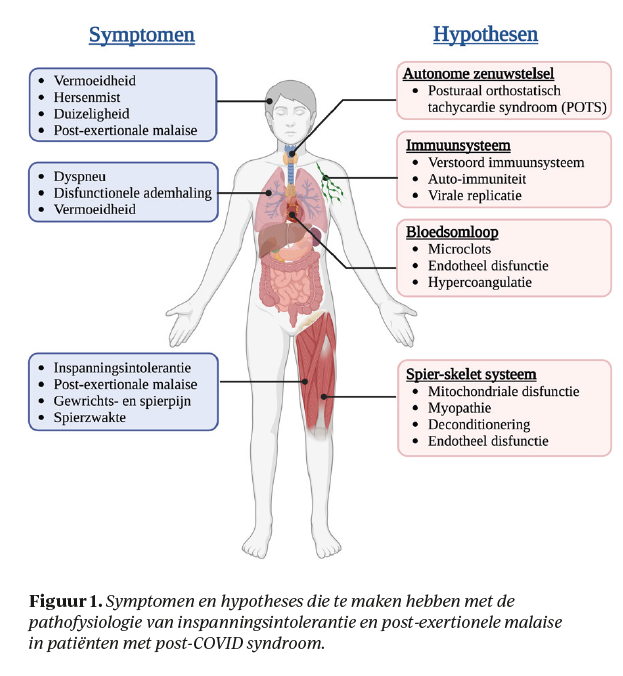
De onderliggende pathologie van vermoeidheid, inspanningsintolerantie en PEM is onbekend. Wetenschappelijk onderzoek suggereert dat de inspanningsintolerantie en PEM in post-COVID syndroom het gevolg kunnen zijn van een combinatie van factoren, namelijk van een verstoring van het immuunsysteem, auto-immuniteit, skeletspieradaptaties, autonome disfunctie en veranderingen in de bloedsomloop.6 Figuur 1 geeft de meest voorkomende symptomen gerelateerd aan vermoeidheid, inspanningsintolerantie en PEM weer, gelinkt aan bovengenoemde hypothesen. In dit artikel bespreken we de pathofysiologie van post-COVID syndroom met specifieke aandacht voor inspanningsintolerantie en PEM. We gaan dieper in op enkele factoren en geven handvatten om hier in de praktijk inhoud aan te geven.
Pathofysiologie van post-COVID
Immunologische ontregeling en virale persistentie
Immunologische ontregeling speelt waarschijnlijk een belangrijke rol in de pathofysiologie van post-COVID syndroom. Daarnaast kan beperkte fysieke activiteit in combinatie met aanhoudende systemische immuunrespons bijdragen aan deconditionering en de verdere ontwikkeling van inspanningsintolerantie. Verschillende studies laten een verstoorde immuunrespons zien in patiënten met post-COVID syndroom, zoals een verhoogde activatie van aangeboren (innate) immuuncellen, een verminderd aantal naïeve T- en B-cellen en hogere cytokine concentraties.6 Sommige onderzoeken vinden autoantilichamen in patiënten met post-COVID syndroom, waardoor vermoed wordt dat post-COVID syndroom een auto-immuunziekte is.6 Toekomstig onderzoek moet uitwijzen wat de link met spierpijn in post-COVID syndroom is. Het is daarnaast onbekend hoe fysieke of cognitieve inspanning het immuunsysteem extra kan activeren, wat de symptomen van PEM zou kunnen verklaren.
Een andere hypothese is dat het virus nog steeds aanwezig is in het lichaam, zelfs nadat de acute fase van de ziekte voorbij is. Virale eiwitten en RNA zijn gevonden in de longen, hersenen, het cardiovasculaire systeem en in spierweefsel, maar onbekend is of dit levend (deelbaar) virus is.7 Persisterende virale reservoirs en de reactivatie kunnen, wellicht in combinatie met auto-immuniteit, leiden tot een aanhoudende inflammatoire weefselreactie, wat kan leiden tot spierzwakte en spierpijn. Deze hypothese is echter nog niet wetenschappelijk aangetoond.
Mitochondriale en endotheel disfunctie
Onderzoek toont aan dat de lagere maximale zuurstofopnamecapaciteit in patiënten met post-COVID syndroom voor een deel verklaard wordt door perifere veranderingen in het spier-skeletsysteem.8,9 Tevens zijn er myopathologische veranderingen waargenomen in het spierweefsel van patiënten met post-COVID syndroom.10 Daarnaast wordt verondersteld dat het virus of de auto-antilichamen mitochondriën kan beschadigen, wat leidt tot een verminderde energieproductie wat de symptomen van vermoeidheid zou kunnen verklaren. Ook speelt endotheel disfunctie, bloedplaatjes activatie en hypercoagulatie een rol in de ziekte,11 maar een causaal verband is niet aangetoond. Tot slot tonen verschillende studies de aanwezigheid aan van microclots in het bloed van patiënten met acute COVID-19 en post-COVID syndroom.12–14 In deze microclots worden auto-antilichamen gevonden.14 De causale relatie tussen auto-immuniteit, endotheeldisfunctie en microclots is nog niet wetenschappelijk aangetoond. Ook is onduidelijk of een herstelbehandeling op basis van deze factoren12 bij alle patiënten een even groot effect op het verminderen van de inspanningsintolerantie en PEM zal laten zien. Deze resultaten laten zien dat de pathofysiologie van inspanningsintolerantie en PEM in patiënten met post-COVID syndroom multifactorieel is en niet alleen verklaard kan worden door deconditionering.
Disfunctionele ademhaling
Tot nu toe zijn er geen duidelijke aanwijzingen dat er sprake is van longschade in niet-gehospitaliseerde patiënten met post-COVID syndroom. Wel laat onderzoek zien dat een disfunctionele ademhaling voorkomt in één op de drie patiënten met post-COVID syndroom.15 Oppervlakkige of snelle ademhaling, hyperventilatie, paradoxale borstbewegingen en overmatig gebruik van hulpademhalingsspieren kunnen resulteren in een versnelde vermoeidheid van ademhalingsspieren en symptomen zoals kortademigheid, vermoeidheid, en inspanningsintolerantie. De causale relatie tussen disfunctionele ademhaling en PEM is nog onbekend.
Discussie en aanbevelingen voor de praktijk
Het post-COVID syndroom heeft grote maatschappelijke implicaties en patiënten hebben grote behoefte aan een behandeling. Helaas is tot op heden nog geen universele herstelbehandeling beschikbaar. Het groeiend aantal patiënt-initiatieven speelt een cruciale rol bij het vergroten van het bewustzijn en het bevorderen van biomedisch onderzoek naar post-COVID syndroom. Patiënten delen via online platforms en sociale media-groepen hun ervaringen met (experimentele) behandelingen, en worden regelmatig gewaarschuwd voor PEM na fysieke training.
Lichaamsbeweging is heilzaam is voor patiënten met chronische aandoeningen, maar (sub)maximale inspanning lijkt gecontraindiceerd te zijn voor patiënten met post-COVID syndroom. De drempel waarboven PEM ontstaat is voor elke patient met PEM anders, en kan op een zeer laag inspanningsniveau liggen. Fysieke en cognitieve inspanning kan leiden tot overmatige vermoeidheid, kortademigheid en verergering van symptomen. Het is daarom van groot belang om in kaart te brengen of een patiënt PEM ervaart, door het afnemen van de DSQ-PEM vragenlijst. Dit kan gebruikt worden in combinatie met andere diagnostische criteria voor ME/CVS. In patiënten zonder PEM draagt fysieke revalidatie hoogstwaarschijnlijk bij aan het herstel, omdat andere factoren ten grondslag liggen aan de verminderde inspanningstolerantie.
‘De slogan ‘Exercise is Medicine’
geldt niet voor patiënten met
post-COVID syndroom’
Wees terughoudend in het afnemen van een maximale inspanningstest, aangezien herstel hiervan voor patiënten met PEM soms weken tot maanden kan duren,1 en het dagelijks leven ernstig belemmert. De diagnostische waarde van een maximaaltest is minimaal, maar een submaximale inspanningstest kan informatie geven op welke intensiteit (c.q. hartslag) PEM geïnduceerd wordt. Deze informatie kan in het dagelijks leven en tijdens beweeginterventies gebruikt worden.16 Pacing-technieken kunnen helpen bij het voorkomen van PEM. Pacing houdt in dat activiteiten en rustperiodes zorgvuldig worden afgewisseld met als doel om de klachten te stabiliseren en te verminderen, en vooral om PEM te voorkomen. Een stappenteller, in combinatie met een hartslagmeter en een activiteitendagboek, kan ingezet worden om een beeld te krijgen van het intensiteitsniveau waarop de patiënt PEM ontwikkelt. Hartslagmonitoring tijdens dagelijkse taken kan als hulpmiddel fungeren door verergerde symptomen aan de hartslag te koppelen (met een vertraging van één tot twee dagen) en daarmee uiteindelijk PEM te voorkomen. De Vereniging voor Sportgeneeskunde heeft een richtlijn uitgebracht met additionele adviezen voor het herstel van fysieke fitheid.16 Een ergotherapeut kan een rol vervullen door patiënten te ondersteunen bij het inzicht in de balans tussen belasting en belastbaarheid en bij klachtenafname geleidelijk uitbreiden van activiteiten. Intensieve fysieke inspanning is niet aan te bevelen als behandeling voor patiënten met post-COVID syndroom: totdat er een herstel-behandeling ontwikkeld is, moeten patiënten een nieuwe energiebalans vinden waarbij PEM wordt voorkomen. Het is nog te vroeg om om op basis van de huidige stand van de wetenschap een herstelbehandeling aan te bieden, omdat er nog veel onduidelijk is over het causale verband tussen microclots, mitochondriale disfunctie en virale persistentie, en het ontstaan van PEM. Er is meer biomedisch onderzoek nodig om te bepalen wat de precieze triggers voor PEM zijn, omdat ook mentale uitputting klachten kan verergeren.
Conclusie
De slogan Exercise is Medicine geldt niet voor patiënten met post-COVID syndroom. Een persoonlijk traject afgestemd op het voorkomen van post-exertionele malaise lijkt vooralsnog de juiste aanpak in deze patiëntenpopulatie. Verder onderzoek is nodig om de specifieke mechanismen te begrijpen die ten grondslag liggen aan inspanningsintolerantie en post-exertionele malaise in patiënten met post-COVID syndroom en ME/CVS.
Dankwoord
De auteurs bedanken Anil van der Zee voor zijn bijdrage aan de tekst.
Vragenlijst over post-exertionele malaise
Om in kaart te brengen of een patiënt post-exertionele malaise ervaart, kan de DSQ-PEM vragenlijst gebruikt worden. Deze vragenlijst kan worden afgenomen door een ervaren behandelaar zoals een arts, fysiotherapeut of ergotherapeut.
Referenties
- Stussman B, Williams A, Snow J, et al. Characterization of Post–exertional Malaise in Patients With Myalgic Encephalomyelitis/Chronic Fatigue Syndrome. Front Neurol 2020;11:1-17.
- Chu L, Valencia IJ, Garvert DW, et al. Deconstructing post-exertional malaise in myalgic encephalomyelitis/chronic fatigue syndrome: A patient-centered, cross-sectional survey. PLoS One 2018;13(6):1-18.
- Komaroff AL, Lipkin WI. ME/CFS and Long COVID share similar symptoms and biological abnormalities: road map to the literature. Front Med 2023;10:1-24.
- National Institute for Health and Care Excellence. Myalgic encephalomyelitis (or encephalopathy)/chronic fatigue syndrome: diagnosis and management. NICE Guidelines, 2021.
- Thaweethai T, Jolley SE, Karlson EW, et al. Development of a Definition of Postacute Sequelae of SARS-CoV-2 Infection. Jama 2023;1-13.
- Davis HE, Mccorkell L, Vogel JM, et al. Long COVID: major findings, mechanisms and recommendations. Nat Rev Microbiol 2023;21:133-46.
- Chen B, Julg B, Mohandas S, et al. Viral persistence, reactivation, and mechanisms of long COVID. Elife 2023;12:1-15.
- Singh I, Joseph P, Heerdt PM, et al. Persistent Exertional Intolerance After COVID-19: Insights From Invasive Cardiopulmonary Exercise Testing. Chest 2022;161(1):54-63.
- Schwendinger F, Knaier R, Radtke T, et al. Low Cardiorespiratory Fitness Post-COVID-19: A Narrative Review. Sport Med 2023;53(1):51-74.
- Hejbøl EK, Harbo T, Agergaard J, et al. Myopathy as a cause of fatigue in long-term post-COVID-19 symptoms: Evidence of skeletal muscle histopathology. Eur J Neurol 2022;29(9):2832-41.
- Gorog DA, Storey RF, Gurbel PA, et al. Current and novel biomarkers of thrombotic risk in COVID-19: a Consensus Statement from the International COVID-19 Thrombosis Biomarkers Colloquium. Nat Rev Cardiol 2022;19(7):475-95.
- Kell DB, Laubscher GJ, Pretorius E. A central role for amyloid fibrin microclots in long COVID/PASC: Origins and therapeutic implications. Biochem J 2022;479(4):537-59.
- Pretorius E, Vlok M, Venter C, et al. Persistent clotting protein pathology in Long COVID/Post-Acute Sequelae of COVID-19 (PASC) is accompanied by increased levels of antiplasmin. Cardiovasc Diabetol 2021;20(1):1-18.
- Kruger A, Vlok M, Turner S, et al. Proteomics of fibrin amyloid microclots in long COVID / post-acute sequelae of COVID-19 (PASC) shows many entrapped pro ‑ inflammatory molecules that may also contribute to a failed fibrinolytic system. Cardiovasc Diabetol 2022;1-23.
- Frésard I, Genecand L, Altarelli M, et al. Dysfunctional breathing diagnosed by cardiopulmonary exercise testing in ‘long COVID’ patients with persistent dyspnoea. BMJ Open Respir Res 2022;9(1):1-8.
- Vessem M, Dijkstra J-W, Janssen K, et al. VSG advies medisch specialistische beweegzorg post-COVID-19: herstel fysieke fitheid. Vereniging voor Sportgeneeskunde. Bilthoven; 2022.
Gerelateerde artikelen NTR

Neurologische en neuropsychologische gevolgen van ernstige COVID-19

Patiënten met post-COVID syndroom worden zieker van inspanning
Nazorg en langetermijngevolgen van COVID-19; interim-analyses tot 12 maanden na ziekenhuisontslag in het CO-FLOW cohort

Post-COVID syndroom bij kinderen: klachten en behandelstrategieën
Gerelateerde artikelen Revalidatie Magazine

Vernieuwde aanpak voor revalidatie na IC-opname

Post-COVID-patiënt lijkt op te knappen van rustige revalidatie